| Използвайки Economy.bg, Вие се съгласявате с "Политика за Cookies/Бисквитки" , необходими за пълната функционалност на услугата. [X] |
|
1170 прочитания
И Moderna поиска разрешение за втора бустерна доза
Искането на компанията обхваща всички, навършили 18 години
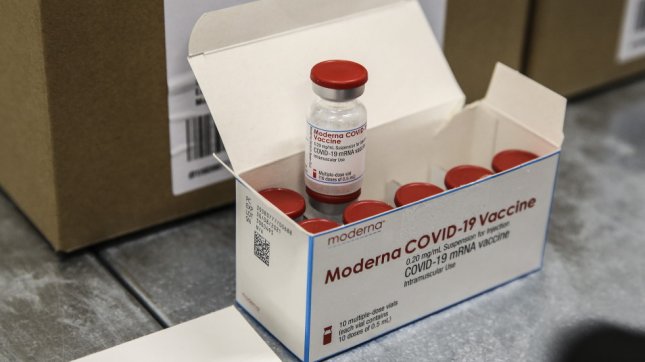 Moderna, Inc. съобщи, че е подала искане до Администрацията по храните и лекарствата на САЩ (FDA) за изменение на разрешението за спешна употреба (EUA), така че да позволи четвърта доза от нейната ваксина срещу Covid-19 (mRNA-1273) при възрастни на 18 и повече години, които са получили първоначален бустер на някоя от разрешените или одобрени ваксини срещу Covid-19. Искането за включване на възрастни над 18 години беше направено, за да се осигури гъвкавост на Центровете за контрол и превенция на заболяванията в САЩ (CDC) и доставчиците на здравни услуги да определят подходящото използване на допълнителна бустер доза mRNA-1273, включително за тези с по-висока риск от Covid-19 поради възраст или съпътстващи заболявания. Това представяне се основава отчасти на наскоро публикувани данни, генерирани в Съединените щати и Израел след появата на Омикрон, уточняват от компанията. FDA на САЩ одобри приложението за лиценз за биологични продукти за SPIKEVAX (иРНК ваксината срещу Covid-19 на Moderna) за предотвратяване на Covid-19 при лица на 18 и повече години на 31 януари 2022 г. Преди това ваксината на Moderna срещу Covid-19 беше налична съгласно EUA в САЩ от 18 декември 2020 г. Бустерна доза от 50 µg е разрешена за спешна употреба в САЩ съгласно EUA за възрастни над 18 години. Трета доза от ваксината Moderna при количество на доза от 100 µg е разрешена за спешна употреба при имунокомпрометирани лица на 18 или повече години в Съединените щати, които са претърпели трансплантация на солидни органи или са диагностицирани със състояния, които се считат за еквивалентни на имунокомпрометиране. Moderna продължава да събира и наблюдава реални данни за своята ваксина срещу Covid-19. Доказателствата от реалния свят продължават да потвърждават ефективността и стабилния профил на безопасност на ваксината. Продължават клинични изпитвания за Омикрон-специфичен бустер на Moderna (mRNA-1273.529) и двувалентен Омикрон-специфичен бустер (mRNA-1273.214). SPIKEVAX (иРНК ваксина срещу Covid-19) е ваксина, показана за активна имунизация за предотвратяване на коронавирусна болест 2019 (Covid-19), причинена от тежък остър респираторен синдром на коронавирус 2 (SARS-CoV-2) при лица на 18 и повече години. По-рано тази седмица и Pfizer поиска разрешение от FDA за 4-та доза от своята ваксина, но искането обхваща само лицата над 65 години.
|
Искам да се абонирам за седмичния бюлетин на Economy.bg:
* Въведеният имейл се използва само за целите на абонамента, имате възможност да прекратите абонамента по всяко време.
|
|
|
|
Copyright © 2024 economy.bg. Издание
на jobs.bg
|